Des scientifiques créent de nouvelles technologies de thérapie génique. Mais peuvent-elles servir pour la SLA ?
20-07-2017
Une nouveau vecteur génétique pourrait permettre d’accroître l’efficacité des thérapies génétiques en cours d’élaboration pour la SLA. Le virus adéno-associé AAV-PHP.eB, développé par une équipe de chercheurs dirigée par les Prof Benjamin Deverman et Viviana Gradinaru à la California Institute of Technology, pénètre dans le système nerveux central, y compris les neurones et les astrocytes.
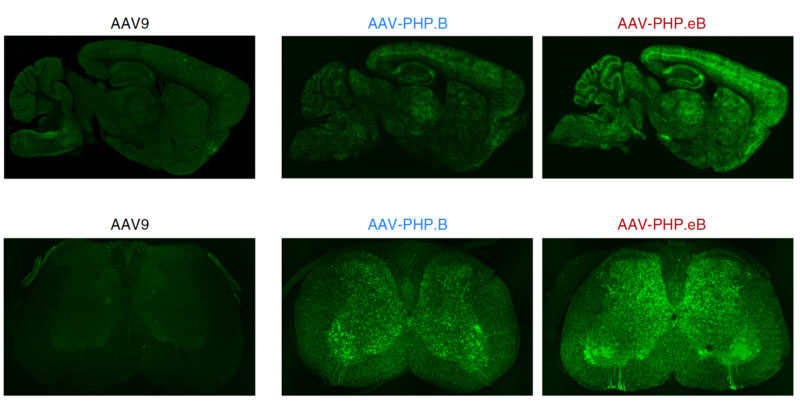
Un transport jusque dans les motoneurones des patients SLA? Selon une analyse préclinique, le vecteur AAV-PHP.eB transporte des gènes dans le cerveau (rangée du haut) et la moelle épinière (rangée du bas) environ 2 fois plus efficacement que les AAV-PHP.B. Un deuxième gène vecteur de transport, connu sous le nom de AAV-PHP.S, qui peut être administré en même temps, pénètre dans le système nerveux périphérique, y compris les muscles. [Reproduit avec l’aimable autorisation de Chan et al., 2017., 2017, Nature Neuroscience]
De plus, le vecteur, dérivé du AAV-PHP.B, peut transmettre, selon une analyse préclinique, plus de 50 % de ces cellules à l’aide de doses au moins 10 fois plus faibles (environ 4 à 5 x 1012 génomes/ kg) et est donc plus adapté aux applications cliniques.
L’étude a été publiée le 26 juin dans la revue Nature Neuroscience.
Le vecteur transporteur de gènes, identifié par un procédé de sélection relatif aux capsides appelé Cre recombinase-based AAV selection, est l’un des vecteurs en nombre croissant en cours d’élaboration afin d’offrir des thérapies potentielles pour des maladies neurologiques du cerveau et de la moelle épinière. Cette stratégie de sélection, appelée CREATE, est la même approche utilisée, en collaboration avec la startup ‘Voyager Therapeutics’ de Boston ( Massachusetts), pour élaborer des vecteurs pour un traitement potentiel de la SLA liée SOD1. La thérapie génétique, appelée VY-SOD101, se trouve au stade préclinique.
Les chercheurs ont utilisé précédemment CREATE pour identifier l’AAV-PHP. B, un vecteur estimé être au moins 40 fois plus efficace que l’émergent vecteur de thérapie génétique AAV9 pour le transport de gènes dans le cerveau et dans la moelle épinière (Deverman et al., 2016;).
Maintenant, l’équipe de Cal Tech espère créer un vecteur de thérapie génétique qui permettra également de transmettre des gènes à d’autres cellules-clé du cerveau et de la moelle épinière, y compris des oligodendrocytes. Ces cellules-clé de soutien, qui peuvent stimuler l’offre d’énergie dans les motoneurones sous stress, dégénèrent aussi en cas de SLA, ce qui pourrait contribuer à la maladie (Nave, 2010; Lee et al., 2012; Kang et al., 2013; Ferraiuolo et al., 2016)
Pendant ce temps, en France, des chercheurs mettent au point une nouvelle approche génétique ciblée afin de réduire la toxicité des motoneurones pour la SLA liée SOD1. La stratégie, axée sur l’ AAV10, consiste en une injection dans le cerveau et le système vasculaire et fait taire le gène SOD1 à l’aide d’un mécanisme ‘U7-mediated exon skipping’ (Biferi et al., 2017). L’approche, selon une analyse de 2017, augmente la durée de vie des souris SOD1 G93A jusqu’à plus du double de celle avec des approches actuelles d’interférence RNA. Maintenant, l’équipe du Prof Barkats adapte cette stratégie pour développer des thérapies génétiques pour la SLA liée C9orf72, la forme la plus courante de la maladie.
Traduction : Fabien
Source : The ALS Research Forum


