Gebruik van multimodale medische beeldvorming en klinische biomerkers in presymptomatische dragers van C9orf72 herhalingsexpansies
20-05-2020
Joke De Vocht, Jeroen Blommaert, Martijn Devrome, Ahmed Radwan, Donatienne Van Weehaeghe, Maxim De Schaepdryver, Jenny Ceccarini, Ahmadreza Rezaei, Georg Schramm, June van Aalst, Adriano Chiò, Marco Pagani, Daphne Stam, Hilde Van Esch, Nikita Lamaire, Marianne Verhaegen, Nathalie Mertens, Koen Poesen, Leonard H. van den Berg, Michael A. van Es, Rik Vandenberghe, Mathieu Vandenbulcke, Jan Van den Stock, Michel Koole, Patrick Dupont, Koen Van Laere, Philip Van Damme
Kernpunten
Vraag
Kunnen metabolische veranderingen in het brein worden gedetecteerd in presymptomatische individuen die drager zijn van een hexanucleotide herhaalexpansie in het C9orf72 gen (preSxC9) door gebruik te maken van time-of-flight fluorine 18–gemerkte fluorodeoxyglucose positron emissie tomografie en magnetische resonantie imaging, en wat is het verband tussen de mutatie en klinische- en vloeistofbiomerkers bij amyotrofische laterale sclerose en frontotemporale dementie?
Bevindingen
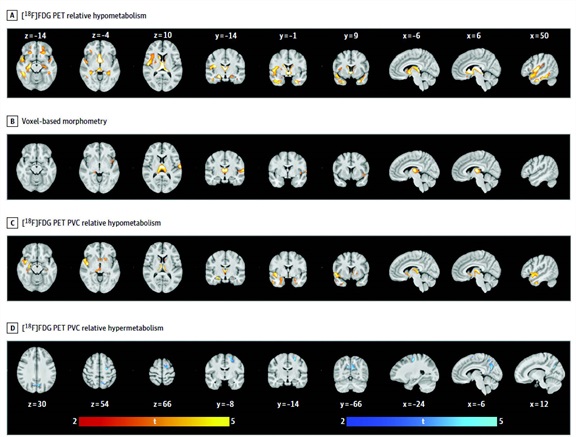
In een case-control studie waaraan 17 preSxC9 individuen en 25 gezonde controles deelnamen, werden via fluorine 18–gemerkte fluorodeoxyglucose positron emissie tomografie significante clusters waargenomen van relatief hypometabolisme in frontotemporale regio’s, de insulaire cortices, basale ganglia, en thalami in de preSxC9 deelnemers. Het gebruik van deze strategie stelde in staat om veranderingen te detecteren op een individueel niveau.
Betekenis
Veranderingen in glucose metabolisme blijken vroeg voor te komen in de volgorde van gebeurtenissen die leiden tot manifestatie van amyotrofische laterale sclerose en frontotemporale dementie. Fluorine 18–gemerkte fluorodeoxyglucose positron emissie tomografie kan een gevoelige biomerker zijn van de presymptomatische fase van de ziekte.
Abstract
Belang
In deze tijd waarin mogelijke nieuwe behandelingsstrategieën zich aanbieden, wordt vroege opsporing van ziektemanifestaties op een individueel niveau in presymptomatische dragers van een hexanucleotide herhalingsexpansie in het C9orf72 gen (preSxC9) in toenemende mate relevant.
Objectieven
Het evalueren van veranderingen in glucose metabolisme voorafgaand aan het begin van symptomen van amyotrofische laterale sclerose of frontotemporale dementie in preSxC9 door gelijktijdig gebruik te maken van fluorine 18–gemerkte fluorodeoxyglucose ([18F]FDG positron emissie tomografie (PET) en magnetische resonantie imaging (MRI), evenals het verband tussen de mutatie en klinische- en vloeistofbiomerkers.
Ontwerp, opstelling, en deelnemers
Een prospectieve case-control studie includeerde 46 deelnemers tussen 30 november 2015 en 11 december 2018. De studie werd uitgevoerd aan het neuromusculair referentiecentrum van de Universitaire Ziekenhuizen Leuven, Leuven, België.
Belangrijkste uitkomsten en metingen
Gegevens van neurologische beeldvorming werden ruimtelijk genormaliseerd en geanalyseerd op het voxel niveau met een hoogtedrempel van P < .001, cluster-niveau volgens familie gecorrigeerde foutmarge van P < .05, en statistische significantie ingesteld op P < .05 voor de volume-of-interest niveau analyse, gebruik makend van Benjamini-Hochberg correctie voor meervoudige correctie. W-score mappen werden berekend door gebruik te maken van individuen die als controle dienst doen als een referentie om de graad van [18F]FDG PET abnormaliteit te kwantificeren. De drempel voor abnormaliteit op de W-score mappen was bepaald als een absolute W-score groter dan of gelijk aan 1.96. Neurofilament niveaus en prestaties op cognitieve en neurologische onderzoeken werden bepaald. Alle hypothesetests waren 1-zijdig.
Resultaten
Van de 42 ingesloten deelnemers waren er 17 met de preSxC9 mutatie (12 vrouwen [71%]; gemiddelde [SD] leeftijd 51 jaar [9]) en 25 gezonde controles (12 vrouwen [48%]; gemiddelde [SD] leeftijd 47 jaar [10]). Vergeleken met controle deelnemers, werden significante clusters van relatief hypometabolisme gevonden in frontotemporale regio’s, basale ganglia, en thalami van preSxC9 deelnemers en relatief hypermetabolisme in de peri-Rolandic regio, superieure frontale gyrus, en precuneus cortex. W-score frequentiemappen toonden gereduceerd glucose metabolisme met locale maxima in de insulaire cortices, centrale operculaire cortex, en thalami in tot 82% van de preSxC9 deelnemers en verhoogd glucose metabolisme in de precentrale gyrus en precuneus cortex in tot 71% van de preSxC9 deelnemers. Andere bevindingen in de preSxC9 groep waren betrokkenheid van de bovenste motor neuronen in 10 deelnemers (59%), cognitieve abnormaliteiten in 5 deelnemers (29%), en verhoogde neurofilament niveaus in 3 van de 16 individuen (19%) die lumbaire punctie ondergingen.
Conclusies en relevantie
De resultaten suggereren dat [18F]FDG PET veranderingen in glucose metabolisme kan aantonen in preSxC9 op een individueel niveau, wat de significante stijging van neurofilament niveaus en het begin van symptomen voorafgaat.
Vertaling: ALS Liga: Dirk
Bron: JAMA Neurology
![]()
Use of Multimodal Imaging and Clinical Biomarkers - JAMA Neurology
Leuvense onderzoekers slagen in vroegtijdige opsporing ALS en frontotemporale dementie
 LEUVEN - Met een specifieke PET-scan zijn onderzoekers verbonden aan de VIB-KU Leuven en UZ Leuven erin geslaagd om bij mensen met mutaties aan het C9orf72-gen hersenveranderingen waar te nemen nog voor ze ziek worden. Volgens neuroloog Philip Van Damme is dit een belangrijke doorbraak die kan helpen bepalen wanneer het het meest opportuun is om te starten met preventieve behandelingen.
LEUVEN - Met een specifieke PET-scan zijn onderzoekers verbonden aan de VIB-KU Leuven en UZ Leuven erin geslaagd om bij mensen met mutaties aan het C9orf72-gen hersenveranderingen waar te nemen nog voor ze ziek worden. Volgens neuroloog Philip Van Damme is dit een belangrijke doorbraak die kan helpen bepalen wanneer het het meest opportuun is om te starten met preventieve behandelingen.
Mutaties aan het C9orf72-gen zijn de meeste voorkomende oorzaak van erfelijke frontotemporale dementie (FTD) en de spierziekte ALS.
FTD is na de ziekte van Alzheimer de meest voorkomende vorm van dementie op jonge leeftijd. De meerderheid van de ALS-patiënten sterft binnen de twee tot vijf jaar na de eerste symptomen.
Dat deze genmutatie leidt tot deze twee uiteenlopende ziekten doet volgens Van Damme vermoeden dat meerdere factoren het ziekteproces in positieve of negatieve zin kunnen beïnvloeden. "Deze factoren zouden interessante therapeutische doelwitten kunnen zijn", aldus de neuroloog.
Joke De Vocht van het labo van Van Damme bestudeerde bij dragers van de vermelde genmutatie met behulp van geavanceerde beeldvorming (geavanceerde time-of-flight 18F FDG-PET MR beeldvorming) de presymptomatische ziektefase en slaagde erin op individueel niveau veranderingen te identificeren nog vooraleer de eerste tekenen van de ziekte opduiken.
Verwijzend naar de nieuwe behandelstrategieën die in ontwikkeling zijn om de ziekte te vertragen of zelfs voorkomen is deze doorbraak volgens Van Damme erg belangrijk. "Dit kan helpen bepalen wanneer het het meest opportuun is om in te grijpen met preventieve behandelingen", aldus de neuroloog.
Bron: MediQuality
PET-scans wijzen op vroege tekenen van glucosemetabolismewijzigingen bij asymptomatische mutatiedragers voor ALS en frontotemporale degeneratie
16-07-2020
Ingekort artikel
PET-scans van asymptomatische dragers van de hexanucleotide herhalingsexpansie in het chromosoom 9 open reading frame 72-gen — die betrokken is bij zowel amyotrofische laterale sclerose als frontotemporale degeneratie — vertoonden veranderingen in het glucosemetabolisme. De bevindingen suggereren dat deze wijzigingen op vroege tekenen van deze beide ziektes kunnen wijzen.
Volgens een rapport in het onlinenummer van 18 mei van JAMA Neurology detecteerden PET-scans van asymptomatische dragers van de hexanucleotide herhalingsexpansie in het chromosoom 9 open reading frame 72 (C9ORF72) -gen veranderingen in het glucosemetabolisme, in vergelijking met gezonde controlegevallen.
Mensen met herhalingsexpansies in dit gen ontwikkelen uiteindelijk mogelijk frontotemporale degeneratie (FTD), amyotrofische laterale sclerose (ALS), of beide. De redenen waarom deze mensen één van deze ziektes of beide krijgen, blijven onduidelijk.
Voor onderhavige studie testte het onderzoeksteam asymptomatische dragers van de herhalingsexpansie (van families met gekende mutaties) aan de hand van een aantal biomerkers – hersenscans, klinische en neurologische onderzoeken, neuropsychologische screenings, en neurofilamentniveaus in het cerebrospinaal vocht (CSV) – om na te gaan of zich veranderingen voordeden die tot een beter begrip kunnen leiden van wat er gebeurt tijdens de stadia die voorafgaan aan de ontwikkeling van symptomen.
“Deze studie toont aan dat zich mogelijk een ruim veld van mogelijkheden opent voor diagnostische doeleinden en vroege behandelingen, wanneer die beschikbaar worden”, zeggen Philip Van Damme, MD, PhD, hoofdauteur van de studie, en doctoraal studente Joke De Vocht, MSc, beiden verbonden aan de Universitaire Ziekenhuizen Leuven in België.
“Het bestuderen van de opeenvolging van gebeurtenissen die zich nog voor de klinische ziekteaanvang voordoen zal van kapitaal belang blijken te zijn om tot een beter begrip te komen van de prodromale ziektestadia en om de klinische ziekteverschijnselen te voorspellen”, voegt hij eraan toe.
Deze C9ORF72-mutaties, die voor het eerst werden geïdentificeerd in 2011 door twee onafhankelijk van elkaar opererende teams van wetenschappers van de Mayo Clinic en het National Institute on Aging, zijn goed voor zowat 34 procent van de familiale ALS-gevallen, bijna 6 procent van de sporadische ALS-gevallen, een kwart van de familiale FTD-gevallen en 5 procent van de sporadische FTD-gevallen.
Studiemethodes, bevindingen
Dr. Van Damme begon zowat tien jaar geleden families met C9ORF72-mutaties te bestuderen. Voor de huidige studie, die tussen 2015 en 2018 werd uitgevoerd, screenden hij en zijn collega’s 42 deelnemers aan de studie. 17 van hen waren dragers van de herhalingsexpansie in het C9ORF72-gen. Ze werden vergeleken met 25 gezonde controlegevallen (met een gemiddelde leeftijd van 47). Men neemt aan dat de pathogene expansie van C9ORF72 meer dan 30 herhalingen bedraagt.
De studiesubjecten werden gescand met behulp van FDG-PET en MRI, en de wetenschappers maten het neurofilament lichte ketting (NfL) en het neurofilament zware ketting; deze merkers van neuronale schade kwamen voor in het CSV van 16 van de 17 C9ORF72-mutatiedragers.
De onderzoekers stelden bij zowat 82 procent van de mutatiedragers significant minder glucosemetabolismeactiviteit vast in welbepaalde hersengebieden — meer bepaald in de insulaire en operculaire schors en de thalami.
Bij 71 procent van de C9ORF72-mutatiedragers vonden ze ook verhoogde traceropname in het peri-Rolandisch gebied. Drie deelnemers aan de studie die drager waren van een herhalingsexpansie vertoonden verhoogde NfL-niveaus, maar de verschillen tussen mensen met de mutatie en de gezonde controlegevallen waren niet statistisch significant.
Dr. Van Damme zegt dat verhoogd NfL bij een paar deelnemers geen verrassing was aangezien uit andere studies al is gebleken dat het NfL drie jaar voor er klinische tekenen opduiken over het algemeen verhoogt. Gezien de onvolledige penetrantie van C9ORF72, blijft nog steeds onduidelijk wanneer en zelfs of alle deelnemers klinische symptomen van ALS of FTD zullen ontwikkelen.
Alle C9ORF72-mutatiedragers ondergingen een compleet neurologisch onderzoek en de neuroloog vond milde tekenen van abnormaliteiten van de bovenste motorneuronen bij 12 van de 17 mensen met de mutatie. “Aangezien de aanwezigheid van een Hoffman-reflex of enkelclonus niet noodzakelijk abnormaal is bij jonge mensen, kwamen alleen de aanwezigheid van een trekking van de kaak, een Babinski-reflex, hyperreflexie, en een verhoogde spierspanning in aanmerking voor verdere analyse”, zo schrijven de auteurs.
Vijf van de 17 C9ORF72-mutatiedragers weken af van de norm van de cognitieve testbatterij – het Edinburgh Cognitief en Gedrags-ALS-Screen. Het uitvoerend functioneren was aangetast bij drie mutatiedragers (18 procent) en een andere persoon scoorde laag op verbale vlotheid. Nog iemand anders bleek volgens het geheugensubdomein van het cognitieve screeninginstrument last te hebben van schade.
 “Tegenwoordig wordt klinisch onderzoek met antisense oligonucleotides uitgevoerd op ALS-patiënten met de C9ORF72-mutatie. Als deze onderzoeken een succes blijken te zijn, kunnen we hopelijk aan studies met asymptomatische dragers beginnen te denken.” — DR. PHILIP VAN DAMME
“Tegenwoordig wordt klinisch onderzoek met antisense oligonucleotides uitgevoerd op ALS-patiënten met de C9ORF72-mutatie. Als deze onderzoeken een succes blijken te zijn, kunnen we hopelijk aan studies met asymptomatische dragers beginnen te denken.” — DR. PHILIP VAN DAMME
De FDG-PET-bevindingen wijzen niet alleen op veranderingen op groepsniveau, maar kunnen ook worden beschouwd op individueel niveau. Dit suggereert dat we ze tijdens de preklinische stadia van de ziekte zouden kunnen gebruiken als biomerkers. Dit zal aan belang winnen naarmate antisense oligonucleotides en andere gentherapieën beschikbaar worden om mensen jaren voor de aanvang van de klinische symptomen te behandelen, zegt dr. Van Damme.
Er was geen significant verband tussen de PET-bevindingen en de leeftijd, de bevindingen over de bovenste motorneuronen, cognitieve bevindingen of neurofilamentniveaus. MRI onthulde een betrokkenheid van gelijkaardige gebieden; frequentiebeelden gaven echter weer dat FDG-PET gevoeliger leek. De hypometabolische gebieden die werden aangetroffen bij de asymptomatische studiepatiënten op de PET-scans zijn vergelijkbaar met diegene die werden gevonden op imagingstudies bij symptomatische dragers.
“Het hypometabolische patroon kan erop wijzen dat het gebied minder actief is of dat er sprake is van atrofie”, voegt dr. Van Damme hieraan toe. “Het was interessant vast te stellen dat de cerebrale glucosewijzigingen niet variabeler waren.”
De wetenschappers vermeldden als potentiële verklaring voor het feit dat sommige gebieden op de PET-scans een hypermetabolisch patroon vertoonden dat dit patroon mogelijk een compenserend mechanisme vormt of een respons op neuro-inflammatie.
“We volgen zowat 60 families met een C9ORF72-mutatie”, zegt dr. Van Damme. “Veel familieleden willen een genetische test laten uitvoeren (en wensen advies). Ze willen weten of ze drager zijn van de mutatie. Bepaalde individuen van deze families zijn erg gemotiveerd om deel te nemen aan het onderzoek.”
De onderzoekers zullen families met deze mutaties blijven bestuderen. “Er zijn nog steeds zoveel onbeantwoorde vragen over deze ziekte. We weten dat deze mutatie niet volledig penetrant is. Ik ken een veertiger die de ziekte heeft, maar een van zijn ouders is een tachtiger die drager is van dezelfde mutatie maar geen klinische tekenen van de ziekte vertoont. Het wordt boeiend te ontdekken wat er na verloop van tijd zal gebeuren”, aldus dr. Van Damme.
“Tegenwoordig wordt klinisch onderzoek met antisense oligonucleotides uitgevoerd op ALS-patiënten met de C9ORF72-mutatie. Als deze onderzoeken een succes blijken te zijn, kunnen we hopelijk aan studies met asymptomatische dragers beginnen te denken.”
Gespecialiseerde commentaar
“Voor mensen met een C9ORF72-mutatie (of andere genetische abnormaliteiten die vrijwel zeker zullen leiden tot FTD of ALS als de persoon lang genoeg leeft), hebben we dringend nood aan imaging- en vochtbiomerkers die aangeven wanneer veranderingen die verband houden met de ziekte detecteerbaar beginnen te worden in de hersenen”, zegt Bradford Dickerson, MD, FAAN, directeur van de cel voor frontotemporale aandoeningen aan het Massachusetts General Hospital en professor Neurologie aan de Harvard Medical School.
“Biomerkers zoals glucosehypometabolisme, die ons vertellen dat de hersenen niet normaal functioneren, zullen hopelijk bruikbaar worden om te meten of behandelingen de hersenfunctie kunnen stabiliseren of verbeteren. Momenteel ontwikkelen we klinische studies en we hebben meer van zulke biomerkers nodig.”
William W. Seeley, MD, de professor Neurologie die wordt gesteund door de familie Zander, professor Neurologie en Pathologie, en directeur van de University of California, San Francisco, Neurodegenerative Disease Brain Bank aan het UCSF Memory and Aging Center, voegt hieraan toe: “De belangrijkste vraag die wordt opgeworpen door deze bevindingen – die een voortzetting zijn van eerder werk – is: wanneer doen abnormaliteiten zich voor? Het is verleidelijk aan te nemen dat de bevindingen wijzen op beginnende neurodegeneratie, maar ook een ontwikkelingsimpact van deze levenslange mutatie is een mogelijkheid. Als de veranderingen het resultaat zijn van een abnormale ontwikkeling, zou dit onze denkwijze over en ons gebruik van imagingbiomerkers voor presymptomatische C9ORF72-gendragers kunnen veranderen. Om dit probleem op te lossen, zijn longitudinale studies en studies in een vroege levensfase vereist.”
Vertaling: Bart De Becker
Bron: Neurology Today


